基于間充質幹細胞的溶瘤免疫療法增強了CAR-T細胞的抗腫瘤功能和效果
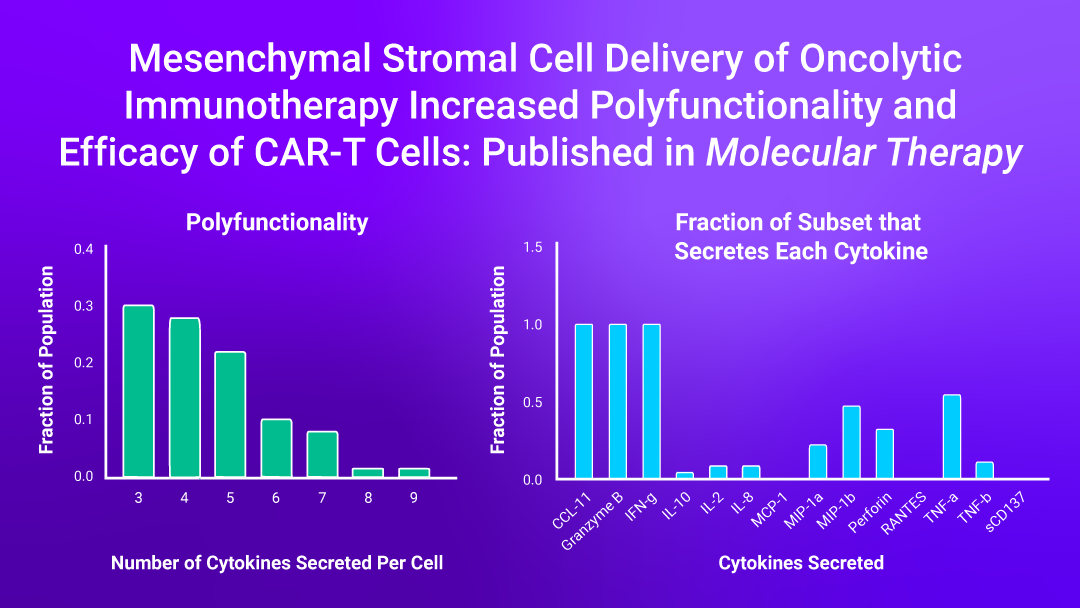
�IsoPlexis單細胞蛋白(bái)組學檢測技術證明了,利用表達IL-12和PD-L1阻斷蛋白(bái)的組合基因工(gōng)程腺病毒感染間充質幹細胞(CAd12_PD-L1 MSCs)促進了HER.2-CAR-T細胞的腫瘤抗原特異性多功能性,并且該多功能性與CAR-T細胞在體(tǐ)外(wài)和體(tǐ)内抗腫瘤活性增強相關。
�單細胞多重蛋白(bái)組學技術也揭示了HER.2 CAR-T細胞的多功能性增加對腫瘤抗原的反應增強,CAd12_PD-L1骨髓間充質幹細胞治療組中(zhōng)有34%的CD4+和40%的CD8+CAR-T多功能性細胞,而HER.2 CAR-T單一(yī)治療組中(zhōng)僅有5%的CD4+和16%的CD8+CAR-T多功能性細胞。
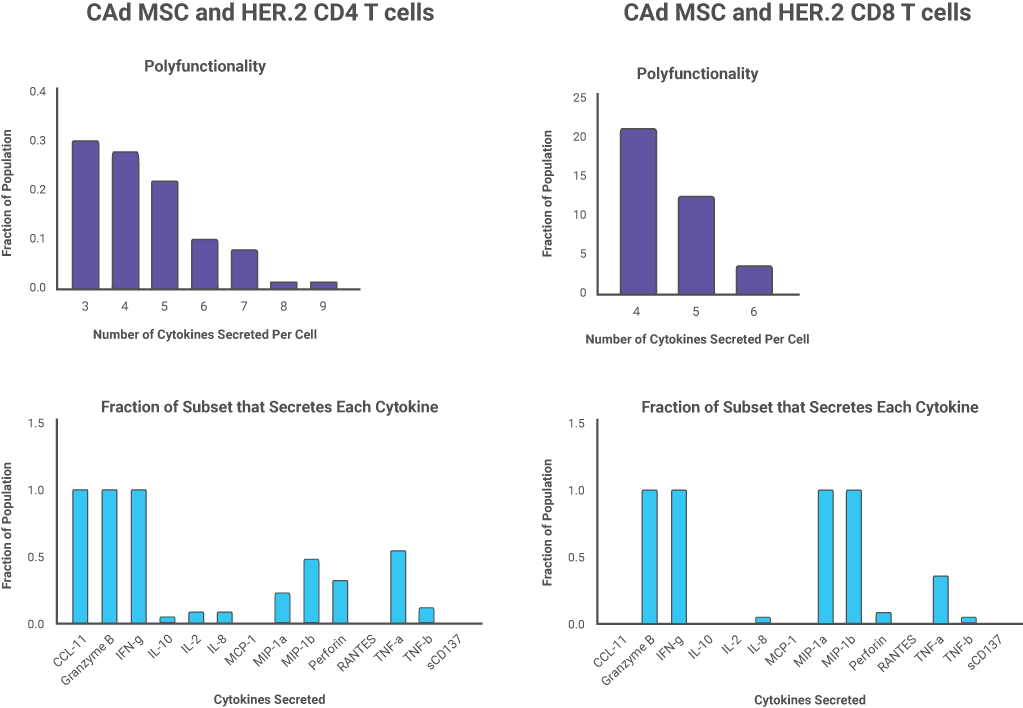
�當腫瘤細胞和CAd12_PD-L1間充質幹細胞MSC載體(tǐ)共培養時,多功能CD4+HER.2 CAR-T細胞顯示出共同分(fēn)泌IFN-g、顆粒酶B和CCL11的大(dà)多數細胞因子的特征,而多功能CD8-HER.2 CAR-T細胞與IFN-g、顆粒酶B、TNF-a和穿孔素共同分(fēn)泌具有更大(dà)的細胞溶解活性,這解釋了CAd12_PD-L1 MSCs提高體(tǐ)内HER.2 CAR-T細胞抗腫瘤活性相關機制。
�IsoPlexis單細胞功能蛋白(bái)質組學技術爲CAd12_PD-L1 MSC在增強HER.2 CAR-T細胞多功能性和效應細胞因子方面提供了獨特的機制見解,并證明了溶瘤免疫療法與CAR-T細胞療法的聯合治療在促進抗腫瘤功能方面的方法學和效果。
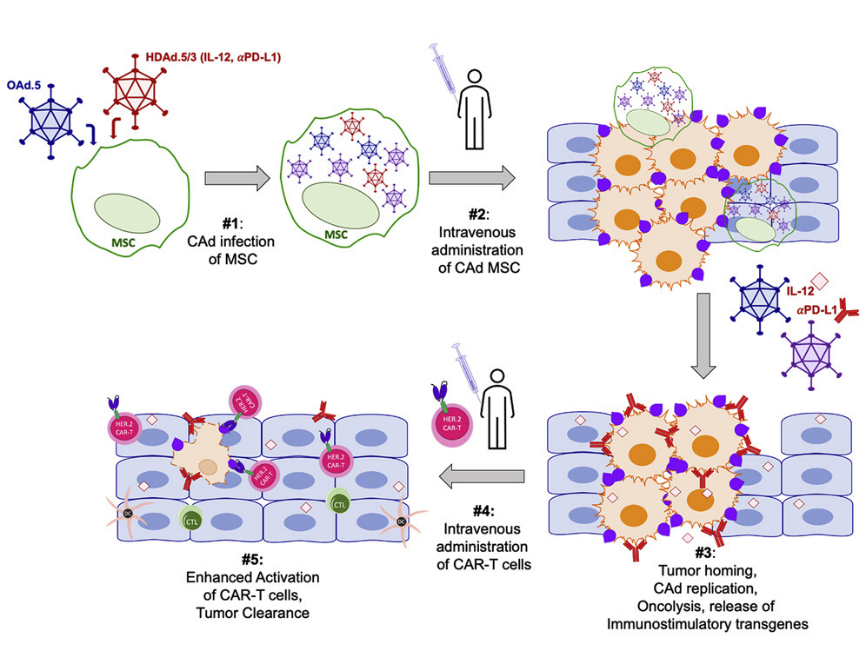
腫瘤微環境 (TME) 的複雜(zá)性可以限制CAR-T細胞的浸潤,并爲使用過繼細胞療法治療實體(tǐ)瘤設置障礙。TME會産生(shēng)免疫抑制蛋白(bái)、細胞因子和趨化因子,從而抑制細胞毒性T細胞反應。因此,确認可破壞TME同時促進T細胞持久性功能驅動因素的療法是實體(tǐ)瘤治療的一(yī)個重要目标。基于工(gōng)程化腺病毒 (OAd) 的溶瘤免疫療法可破壞TME并刺激相關CAR-T細胞,增強宿主抗腫瘤免疫反應。但是溶瘤病毒如何遞送到相應病竈内的腫瘤部位極具挑戰性,而且由于患者對病毒治療的天然或适應性免疫反應,在某些情況下(xià)無法進行靜脈給藥。爲了克服這些挑戰,利用特定細胞載體(tǐ)系統如間充質幹細胞 (MSC) 可将OAd遞送至腫瘤部位。最近發表在Molecular Therapy上的一(yī)項研究通過IsoPlexis的單細胞蛋白(bái)質組學技術證實了OAd細胞遞送聯合CAR-T療法在治療實體(tǐ)瘤方面的方法學及效果。
利用功能性單細胞蛋白(bái)質組學技術解決溶瘤免疫療法破壞腫瘤微環境的挑戰
McKenna等科學家在研究中(zhōng)使用間充質幹細胞(MSCs)系統的遞送包含OAd和輔助性腺病毒(HDAd) 并表達白(bái)介素-12(IL-12)和PD-L1(程序性死亡配體(tǐ)1)阻斷蛋白(bái)的組合載體(tǐ)[CAd]。CAd感染的MSCs可以遞送并釋放(fàng)有功能的病毒感染和裂解肺腫瘤細胞,同時通過釋放(fàng)IL-12和PD-L1阻斷蛋白(bái)增強CAR-T細胞抗腫瘤活性。這種方法與靶向HER2特異性CAR-T細胞療法的結合可在體(tǐ)外(wài)消除了3D培養的腫瘤球體(tǐ),并且在體(tǐ)内則觀察到抑制了兩種原位肺癌模型的腫瘤生(shēng)長。與單一(yī)CAR-T細胞治療相比,組合載體(tǐ)CAd通過間充質幹細胞MSCs遞送療法增加了人T細胞的總體(tǐ)數量,并增強了其多功能細胞因子的分(fēn)泌。
單細胞分(fēn)泌蛋白(bái)質組學鑒定與CAd感染的骨髓間充質幹細胞治療的CAR-T細胞抗腫瘤功能改善相關的上調T細胞多功能性
研究中(zhōng)也提到IsoPlexis的功能蛋白(bái)質組學技術來分(fēn)析CAd感染的MSC提高HER.2 CAR-T細胞功效的機制。單細胞分(fēn)泌組芯片用于測量單個CAR-T細胞的多功能性。在以前的研究中(zhōng),多功能性與抗腫瘤活性有關,并可以很好預測臨床結果。IsoPlexis單細胞分(fēn)泌蛋白(bái)質組學技術發現CAd-MSC與腫瘤細胞系共培養的HER2 CAR-T細胞相比未經CAd-MSC共同培養的CAR-T細胞具有更多的多功能性T細胞(分(fēn)别占CD4+和CD8+細胞的34%和40% VS 5%和16%)。
聯合治療通過增加CAR-T細胞中(zhōng)多功能細胞的數量有效地增強了HER.2 CAR-T細胞的抗腫瘤活性。
在IsoSpeak軟件對相關細胞亞群進行進一(yī)步分(fēn)析中(zhōng)發現,與未感染Ad的MSCs共培養的一(yī)部分(fēn)CD4+細胞主要分(fēn)泌IL-8,而與CAd MSCs共培養的一(yī)個CD4+細胞亞群中(zhōng)細胞分(fēn)泌多達9種細胞因子,其中(zhōng)大(dà)部分(fēn)同時分(fēn)泌IFN-g、Granzyme B和CCL11。CAd MSCs促進了CD4+ CAR-T細胞對腫瘤細胞的促炎細胞因子的産生(shēng)。在CD8+ CAR-T細胞亞群中(zhōng)則發現CD8+ HER.2 CAR-T細胞分(fēn)泌相關效應因子的增多,包含INF-g,Granzyme B,MIP-a等。經CAd MSCs處理的CD4+和CD8+ CAR-T細胞均顯示CCL11的分(fēn)泌增多,(CCL11是一(yī)種與粘附分(fēn)子和T細胞趨化性增加相關的趨化因子)。IsoPlexis功能性單細胞蛋白(bái)質組學技術揭示了CAd MSCs增強CAR-T細胞功效的抗腫瘤活性相關機制。
這種抗腫瘤活性在随後的小(xiǎo)鼠肺癌模型中(zhōng)的實驗結果一(yī)緻,利用IsoPlexis技術可以在更短的時間内利用體(tǐ)外(wài)3D細胞培養模型提供與體(tǐ)内生(shēng)物(wù)學反應相一(yī)緻的結果和見解。CAd-MSCs治療聯合HER.2 CAR-T治療與單獨CAR-T治療相比,能夠顯著抑制腫瘤生(shēng)長。肺部腫瘤内T細胞數據顯示,與單一(yī)CAR-T治療組相比,CAd-MSC聯合CAR-T治療細胞組中(zhōng)CD8+T細胞的耗竭标志(zhì)物(wù)Tim3的表達降低,表明CAd-MSC促進了T細胞的持久性。使用異種移植肺腫瘤模型進行的小(xiǎo)鼠體(tǐ)内研究得出的結果與3D培養細胞中(zhōng)結果相一(yī)緻:聯合治療實現腫瘤在2周内完全清除,且未觀察到任何負面作用。
總結McKenna等人的研究結果揭示了CAd-MSCs和CAR-T獨特的聯合療法的抗腫瘤活性内在機制。聯合治療可破壞TME,改善T細胞浸潤,增強T細胞的多功能性,而多功能性與抗腫瘤活性相關。IsoPlexis通過IsoCode單細胞分(fēn)泌蛋白(bái)組芯片解決方案獨特地揭示了這一(yī)點,該解決方案能夠全自動檢測數千個單細胞中(zhōng)32+種細胞因子數據,相對傳統技術僅捕獲少數功能蛋白(bái),可以在更短的時間内捕獲全系列功能蛋白(bái)。IsoPlexis單細胞和多組學平台爲科學家節省了寶貴的時間和金錢,加速了臨床研究進展。
參考文獻:
1. McKenna et al., Mesenchymal stromal cell delivery of oncolytic immunotherapy improves CAR-T cell antitumor activity, Molecular Therapy (2021)