如何加強CAR-T療效:單CAR雙CAR?二代三代……
衆所周知(zhī),CAR-T結構包括三部分(fēn):
(1)識别靶抗原的胞外(wài)scFv區;
(2)跨膜鉸鏈區;
(3)胞内信号結構域,以介導T細胞信号轉導,引起T細胞活化、擴增和抗腫瘤免疫應答等。
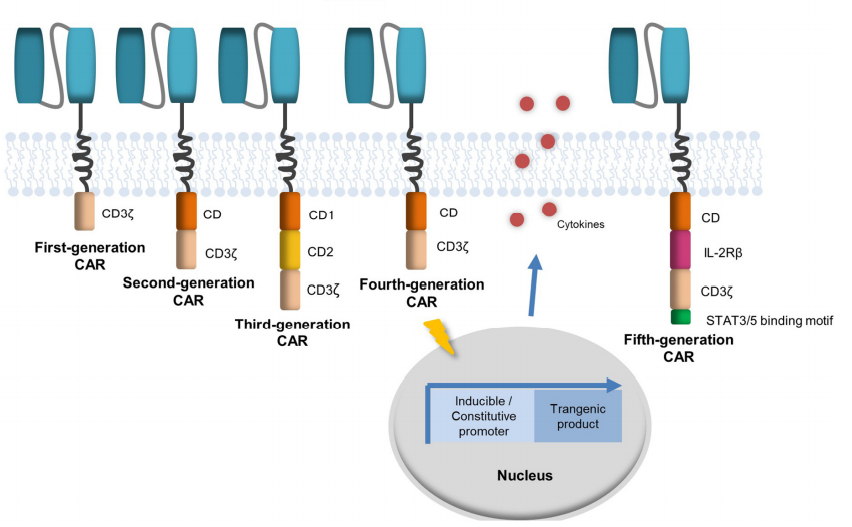
CAR-T細胞療法的發展。(圖片來自Journal of Controlled Release, 2020, 319:246-261.)
其中(zhōng)胞外(wài)區結構決定了CAR的特異性和與靶抗原的結合親和力。随着CAR-T的發展,逐漸發現單靶點CAR-T細胞療效受限于腫瘤抗原的異質性,常出現腫瘤複發的問題,于是近年來逐漸向多靶點CAR-T細胞療法轉變,比如探索CD19/CD20雙特異性CAR治療複發難治性B細胞淋巴瘤等。
另外(wài),胞内結構域近年來也做了不斷優化。從二代CAR開(kāi)始,就加入了不同的共刺激信号結構域,以解決一(yī)代CAR在體(tǐ)内存活時間較短,且活性差的問題。二代CAR-T技術依據不同的共刺激結構域主要分(fēn)爲兩大(dà)類:基于CD28和基于CD137(4-1BB)的共刺激結構域。一(yī)般認爲,CD28所傳遞的活化信号相較于CD137(4-1BB)更強,可使T細胞在較短時間内達到很高的殺傷活性。而CD137(4-1BB)所傳遞的活化信号則會更加持久。
到三代CAR-T同時引入兩個共刺激信号分(fēn)子,以期提高T細胞增殖活性、細胞毒性,并延長T細胞存活時間。第四代CAR-T結構引入了自殺基因、促炎症細胞因子和共刺激配體(tǐ)等,希望達到精細調控和克服腫瘤免疫微環境抑制等目的。
關于如何将CAR-T胞外(wài)和胞内的結構域進行優化,強強聯合,以提高CAR-T的作用,目前仍在探索中(zhōng)。
墨菲特癌症治療及研究中(zhōng)心(H.Lee Moffitt Cancer Center and Research Institute)Marco L Davila博士帶領的研究團隊新近在Journal for ImmunoTherapy of Cancer(影響因子 13.751)發表題爲“4-1BB and optimized CD28 co-stimulation enhances function of human mono-specific and bi-specific third-generation CAR T cells “的研究文章表明,4-1BB和經過優化的CD28共刺激信号可增強三代單特異性CAR和雙特異性CAR的功效,包括細胞擴增、細胞持久性和抗耗竭能力等。

研究方法
作者設計了4-1BB或聯合僅含有PYAP信号基序(mut06)的CD28作爲CD19特異性CAR-T細胞的共刺激信号,通過細胞和分(fēn)子生(shēng)物(wù)學體(tǐ)外(wài)和體(tǐ)内實驗對不同設計結構的CAR-T細胞進行評估,包括:
1、 體(tǐ)外(wài)細胞分(fēn)析:免疫表型、細胞因子分(fēn)泌、實時細胞毒殺傷能力和CAR-T多功能性反應
2、體(tǐ)外(wài)蛋白(bái)定量:Western blot分(fēn)析不同CAR-T的LCK募集情況
3、小(xiǎo)鼠體(tǐ)内腫瘤模型實驗:在NOD scid γ (NSG)小(xiǎo)鼠模型中(zhōng)分(fēn)析CAR-T對Raji細胞腫瘤的控制
此外(wài),作者還結合4-1BB和mut06設計了雙特異性CD20/CD19 CAR,并采取以下(xià)實驗進行評估:
1、多次體(tǐ)外(wài)抗原刺激:分(fēn)析細胞擴增能力、細胞記憶性表型、PD1+CD39+表型(細胞耗竭)
2、小(xiǎo)鼠腫瘤模型:在Raji或Nalm6小(xiǎo)鼠腫瘤模型中(zhōng)研究雙特異性CAR-T細胞清除CD20/CD19腫瘤細胞的能力。
思路理清楚了,我(wǒ)(wǒ)們來看下(xià)研究結果吧~
研究結果
一(yī)、4-1BB和mut06共刺激可提高CAR-T細胞的記憶性表型
爲了評估4-1BB和mut06聯合刺激如何影響CAR功能,研究人員(yuán)一(yī)共設計了5種CAR結構,具體(tǐ)如下(xià):
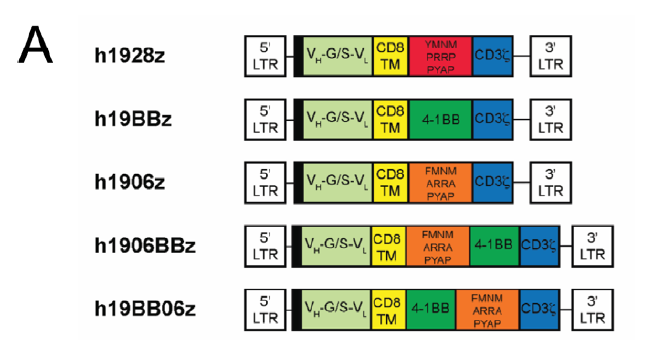
所有CAR結構包括FMC63 scFv胞外(wài)區和CD8α跨膜鉸鏈結構域,不同之處在于胞内的共刺激信号。
wh1906z (mut06):與CD28子結構域相比,h1906z用FMNM和ARRA取代了YMNM和PRRP,隻留下(xià)一(yī)個功能性的PYAP信号基序。
wh1906BBz:在細胞膜近端是mut06結構域,然後依次是4-1BB和CD3ζ。
wh19BB06z:在細胞膜近端是4-1BB結構域,然後依次是mut06和CD3ζ。
将不同設計的CAR-T細胞與靶細胞(3T3-hCD19)以1:10的效靶比共培養24小(xiǎo)時,流式檢測CAR-T細胞表型,結果顯示:
1、 h19BB06z細胞表面的CAR表達水平最高,與靶細胞刺激前趨勢一(yī)緻。
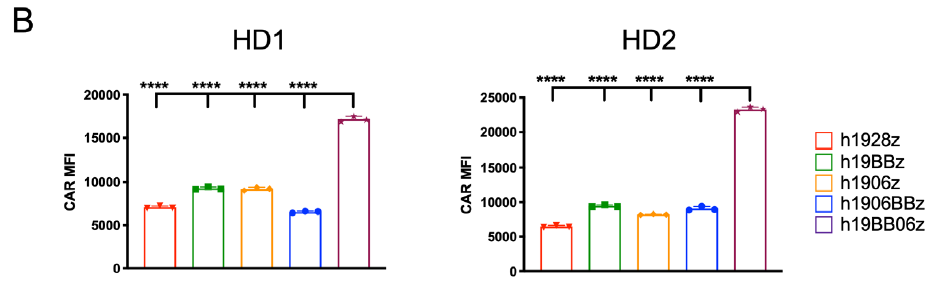
2、 在與靶細胞共培養後,同時含有4-1BB和mut06共刺激信号的CAR-T(h1906BBz和h19BB06z)具有更高的CD4/CD8比例,同樣與靶細胞共培養前的趨勢一(yī)緻。
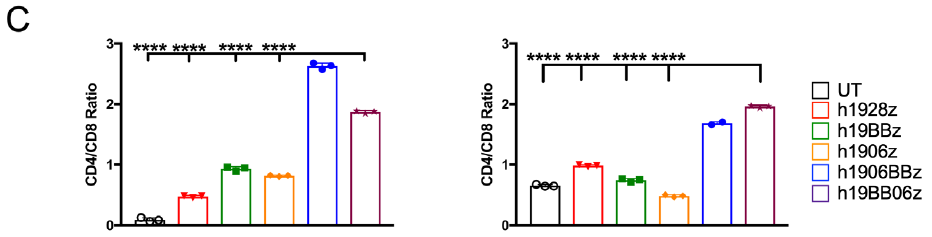
3、在與靶細胞共培養後,同時含有4-1BB和mut06共刺激信号的CAR-T(h1906BBz和h19BB06z)細胞含有更高比例的中(zhōng)央記憶性T細胞(CCR7+CD45RA-)。
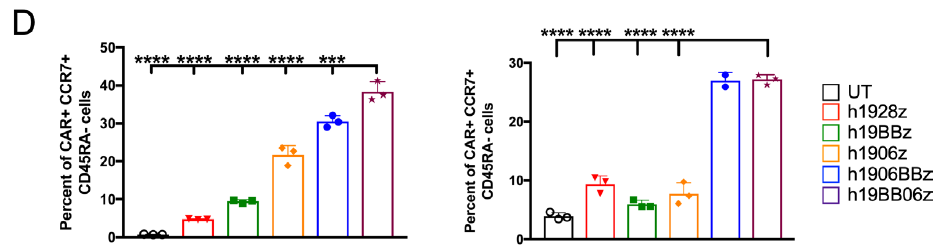
爲了進一(yī)步驗證在更長時間點的細胞分(fēn)化情況,研究人員(yuán)每周用靶細胞刺激CAR–T,共計3周。結果顯示h19BB06z CAR-T細胞能夠保持更持久的高比例中(zhōng)央記憶性細胞表型,而其餘的CAR-T偏向T細胞分(fēn)化表型。
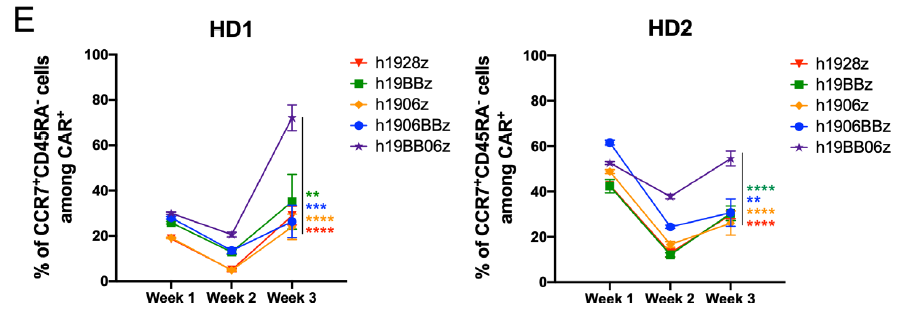
綜上,與其他CAR-T結構相比,h19BB06z CAR-T細胞可以保持更持久、更高水平的中(zhōng)央記憶性細胞表型。
二、4-1BB和mut06共刺激結構域影響h1906BBz和h19BB06z CAR-T細胞的功能
對CAR-T細胞的功能檢測包括細胞因子定量、細胞多功能性檢測、體(tǐ)外(wài)殺傷實驗和胞内信号轉導分(fēn)析。
1、細胞因子檢測
爲了檢查不同CAR的效應功能,研究人員(yuán)将三名健康人來源的CAR-T細胞與靶細胞以1:10的效靶比共培養24小(xiǎo)時,收集上清檢測細胞因子含量。
結果顯示:
wh1906z (mut06)的IFN-γ、IL-2和TNFα水平最低,與CD28結構突變導緻的信号傳導抑制和功能受損有關。
w當4-1BB與mut06共刺激信号聯合時,細胞上清中(zhōng)IFN-γ、IL-2和TNF-α的分(fēn)泌增加,尤其是h19BB06z。
wIL-6的分(fēn)泌與患者的CRS相關,在所有CAR結構中(zhōng)均保持較低水平,除了h19BB06z。

2、細胞多功能性檢測
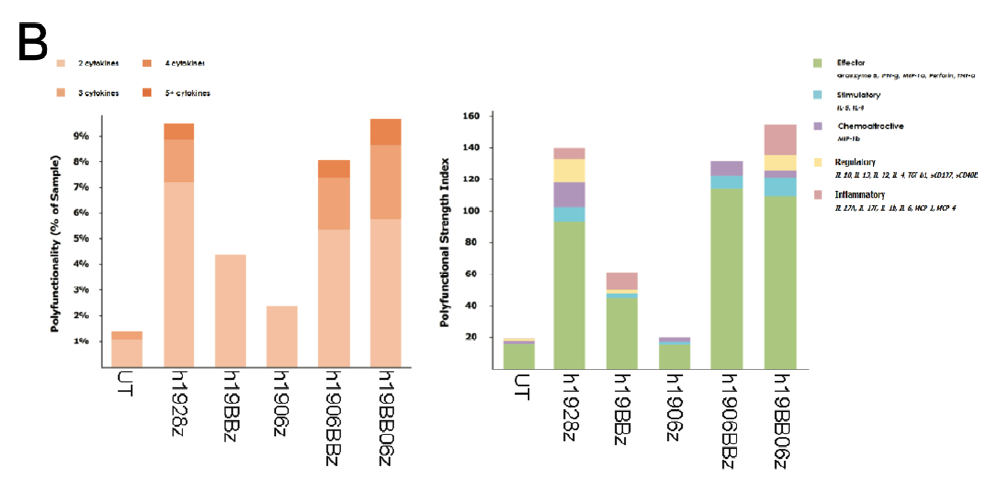
此外(wài),研究人員(yuán)還探索了CAR-T細胞的多功能性,即單個細胞分(fēn)泌兩種及以上細胞因子的能力。已有多項研究表明,CAR-T細胞的多功能性是體(tǐ)内生(shēng)理效應的一(yī)個重要預測指标。爲了驗證這一(yī)點,作者采用微流控芯片,在單細胞水平上分(fēn)析了數百個CAR-T細胞分(fēn)泌的28種細胞因子,包括分(fēn)泌頻(pín)率和細胞因子強度。
将CAR-T細胞與靶細胞共培養4小(xiǎo)時後加載到芯片進行分(fēn)析,結果發現h1928z、h1906BBz和h19BB06z的多功能細胞百分(fēn)比增加。細胞多功能指數(PSI)是衡量CAR-T細胞療效的預測性指标,通過計算多功能細胞的百分(fēn)比乘以所分(fēn)泌的各種細胞因子的強度獲得。采用這一(yī)檢測方法顯示,h1928z、h1906BBz和h19BB06z具有最高的PSI水平。這些數據說明4-1BB和mut06結合可以增強CAR-T細胞的多功能性,與h1928z相當。
3、體(tǐ)外(wài)殺傷能力檢測
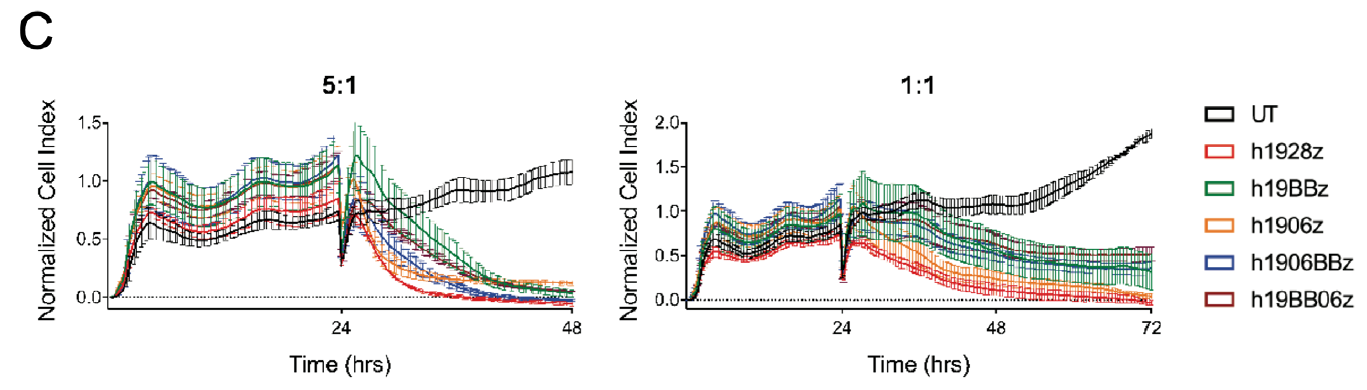
所有CAR-T在兩種效靶比下(xià)(5:1和1:1)都具有快速有效的殺傷作用。這表明體(tǐ)外(wài)細胞毒作用不受共刺激域的選擇或組合的影響。
 4、CAR-T細胞胞内信号轉導分(fēn)析
4、CAR-T細胞胞内信号轉導分(fēn)析
淋巴細胞特異性蛋白(bái)酪氨酸激酶(LCK)是影響CAR-T細胞功能的關鍵信号轉導分(fēn)子。最近有研究表明,LCK募集到4-1BB CARs可以增強CAR-T細胞的細胞毒性。研究人員(yuán)對不同CAR在靶細胞刺激24h後的胞内LCK磷酸化水平進行了分(fēn)析,發現與第二代CARs相比,第三代CARs的pLCK均有所增加。
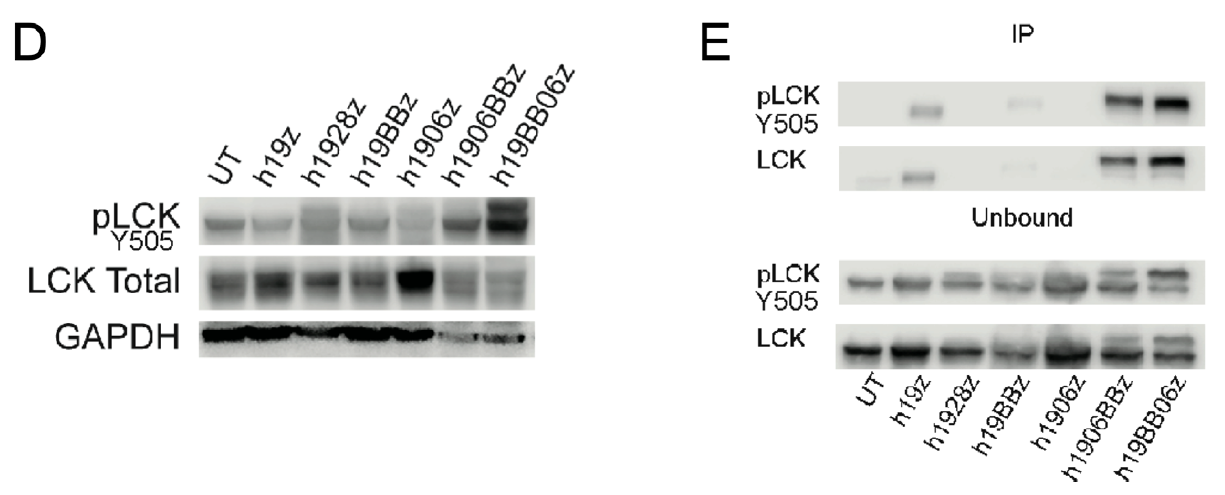 而且,h19BB06z的LCK磷酸化水平最高,說明共刺激域的位置可能會影響pLCK。此外(wài)還發現大(dà)量的pLCK和總LCK與h19BB06z CAR分(fēn)子相關。這些數據表明,h1906BBz和h19BB06z的體(tǐ)外(wài)功能增強是由于pLCK的增加,共刺激區域的定位可影響CAR相關的LCK信号。
而且,h19BB06z的LCK磷酸化水平最高,說明共刺激域的位置可能會影響pLCK。此外(wài)還發現大(dà)量的pLCK和總LCK與h19BB06z CAR分(fēn)子相關。這些數據表明,h1906BBz和h19BB06z的體(tǐ)外(wài)功能增強是由于pLCK的增加,共刺激區域的定位可影響CAR相關的LCK信号。
三、共刺激域定位影響細胞體(tǐ)外(wài)擴增和體(tǐ)内腫瘤殺傷
1、CAR-T體(tǐ)外(wài)持續擴增能力
靶比的靶細胞刺激CAR-T細胞,每7天重複刺激一(yī)次,共計4周,檢測CAR-T細胞反應性。
結果顯示在重複抗原刺激後,h19BB06z CAR - T細胞表現出最強的體(tǐ)外(wài)擴增能力、細胞毒作用和細胞因子分(fēn)泌。
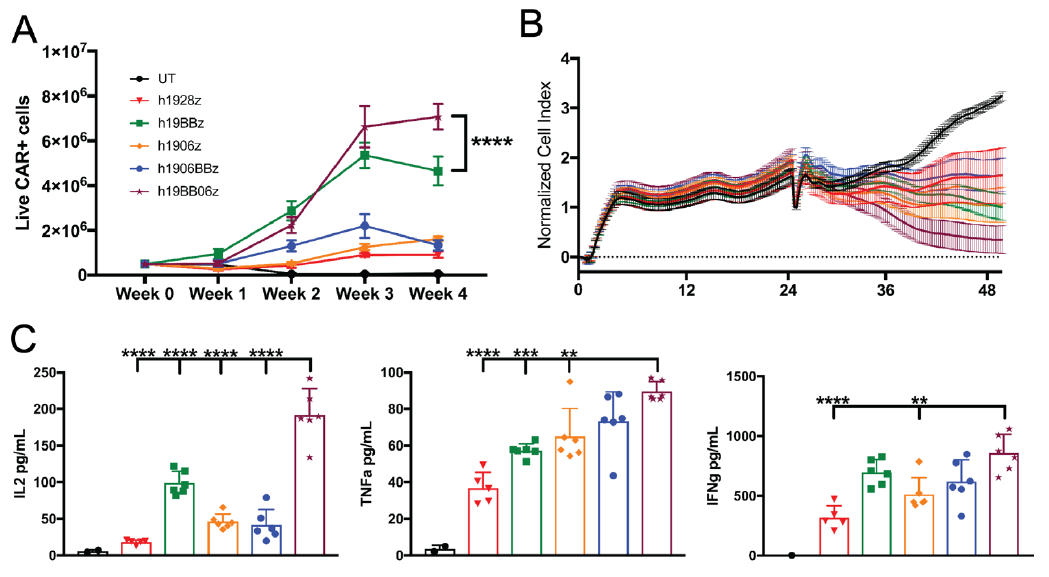
而h1906BBz CAR-T細胞比h19BB06z表現出更低的增殖、細胞毒作用和IL-2的産生(shēng),再次表明共刺激域定位可以影響CAR功能。
2、體(tǐ)内抗腫瘤能力
爲了确定h1906BBz和h19BB06z CAR-T細胞在體(tǐ)内控制腫瘤生(shēng)長的能力,研究人員(yuán)将Raji B淋巴細胞腫瘤細胞注射到NSG小(xiǎo)鼠體(tǐ)内形成腫瘤。結果發現,與UT和h1906BBz相比,h19BB06z CAR-T細胞能夠更好地控制腫瘤生(shēng)長。在接受h19BB06z治療的小(xiǎo)鼠血液中(zhōng),CAR+細胞略有增加,CD19+細胞相應減少。
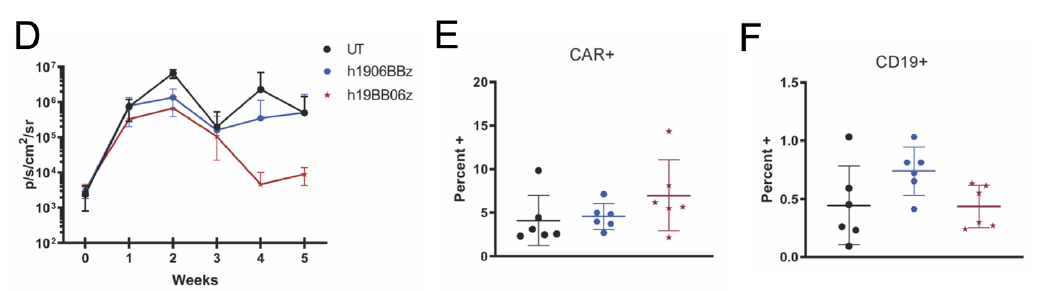
總之,這些數據表明,與h1906BBz相比,h19BB06z CAR-T細胞在體(tǐ)外(wài)增殖、長期細胞毒性和體(tǐ)内腫瘤殺傷能力增強。因此,研究人員(yuán)選擇BB06方向進行進一(yī)步的評估。
四、雙特異性CAR-T研究
後續,研究人員(yuán)開(kāi)發了四種能夠識别人CD19和CD20抗原的雙特異性CAR(結構設計如下(xià)),這種多抗原識别方法在以往研究中(zhōng)發現可以減緩由于腫瘤抗原逃逸引起的疾病複發。而且,這四種CAR-T包含二代或三代CAR結構,以進行深入比較。
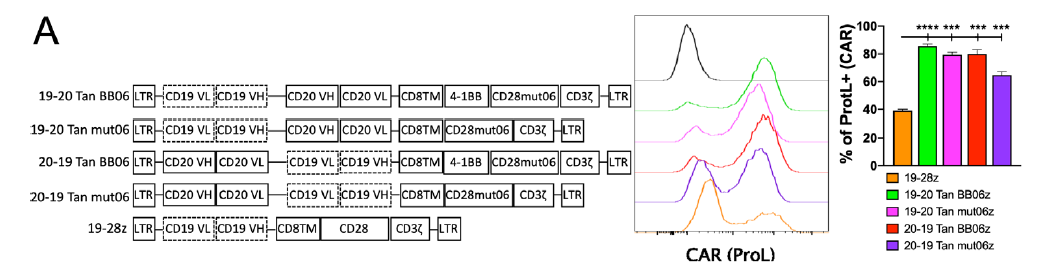
在後續研究中(zhōng),作者依然采用了前文所述的不同研究方法對各種雙特異性CAR-T進行評估和比較,包括細胞表型、細胞因子分(fēn)泌、細胞擴增和體(tǐ)外(wài)/體(tǐ)内腫瘤殺傷能力等。
當然,除了常規細胞評估方法外(wài),作者還采用了IsoPlexis單細胞功能蛋白(bái)組技術來評估細胞多功能性和PSI(細胞多功能指數)哦~
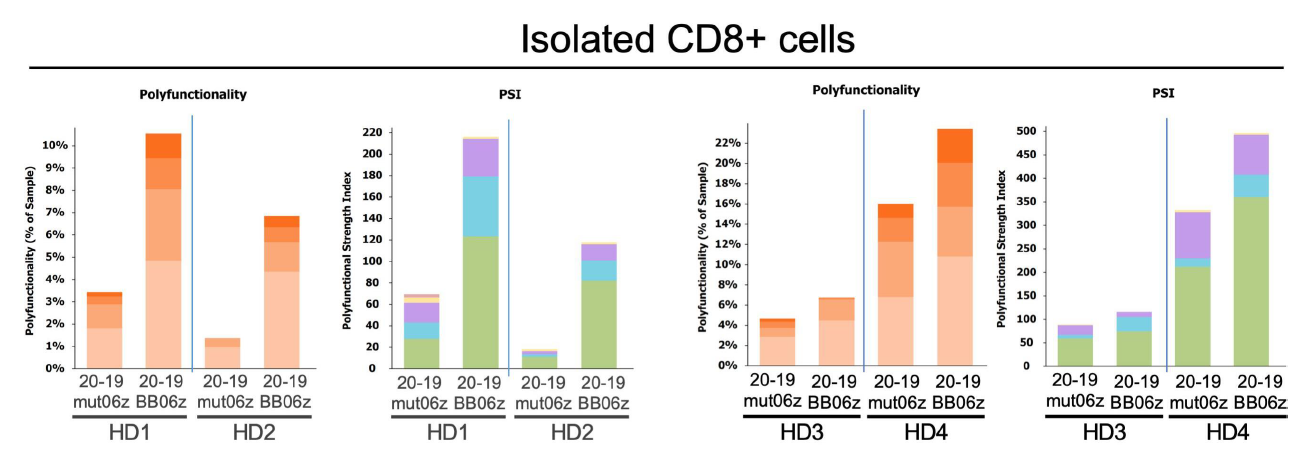
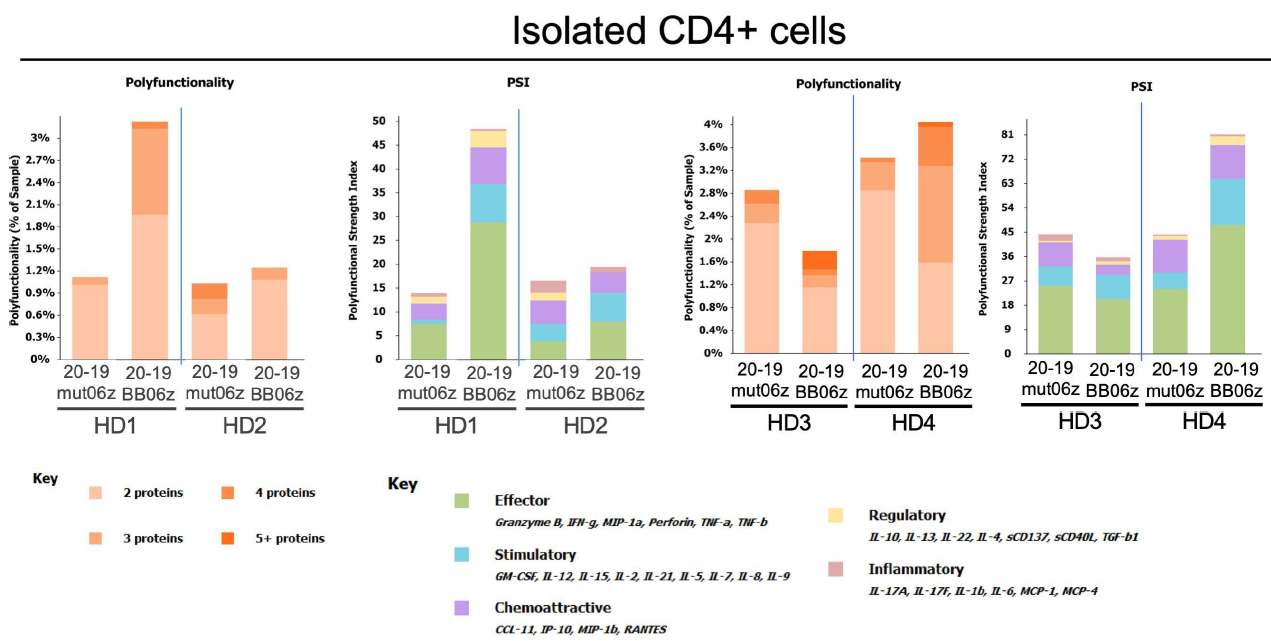
如果感興趣的話(huà),可點擊以下(xià)鏈接即可下(xià)載原文哦:
下(xià)載鏈接:資(zī)料下(xià)載